Thông tin thuốc tháng 02/2026
Báo cáo hoạt động theo dõi adr năm 2025 của Bệnh viện Từ Dũ
1. Tổng quan số lượng báo cáo ADR của Bệnh viện Từ Dũ
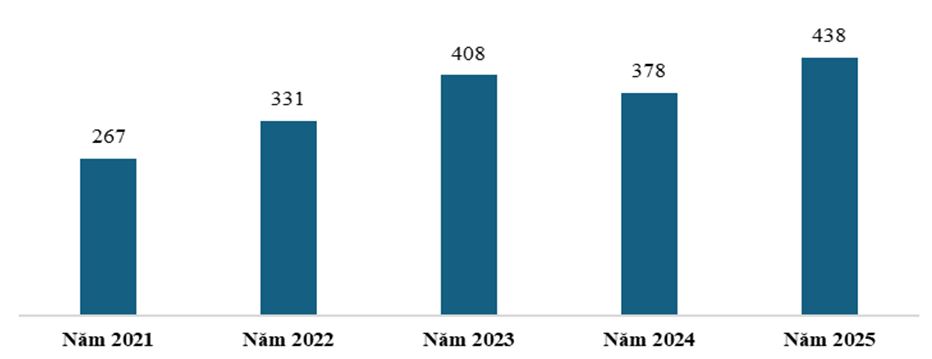
Hình 1. Số lượng báo cáo ADR tại Bệnh viện Từ Dũ giai đoạn năm 2021 - 2025
Trong năm 2025:
- Bệnh viện đã thực hiện 438 báo cáo ADR, tăng 15,9% so với năm 2024 (378 báo cáo), tăng 7,4% so với năm 2023 (408 báo cáo) và cao nhất trong giai đoạn từ năm 2021-2025.
- Số lượng báo cáo ADR ngoại trú là 06 báo cáo, giảm 3 lần so với năm 2024 (18 báo cáo).
- Bệnh viện Từ Dũ được Trung tâm DI&ADR quốc gia xếp hạng 06/1045 cơ sở khám chữa bệnh có hoạt động theo dõi ADR hiệu quả trong báo cáo tổng kết ADR quốc gia vào tháng 7/2025.
1.1. Phân bố báo cáo ADR theo tháng
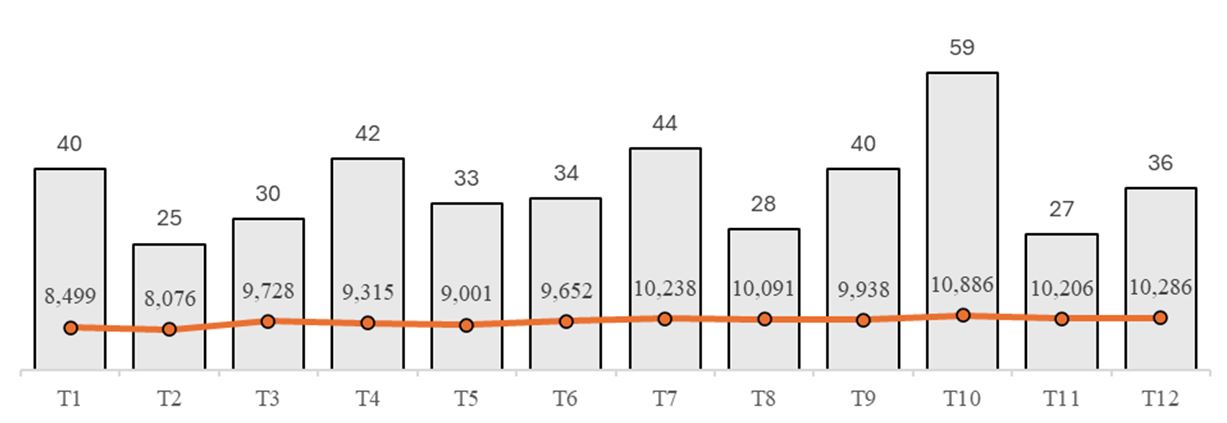
Hình 2. Phân bố báo cáo ADR theo tháng và số lượng bệnh nhân nội trú năm 2025
Tháng 2 và tháng 10 có số lượng bệnh nội trú thấp nhất và cao nhất, tương ứng lần lượt với số lượng báo cáo ADR thấp nhất và cao nhất trong năm 2025.
1.2. Phân bố báo cáo ADR theo khoa
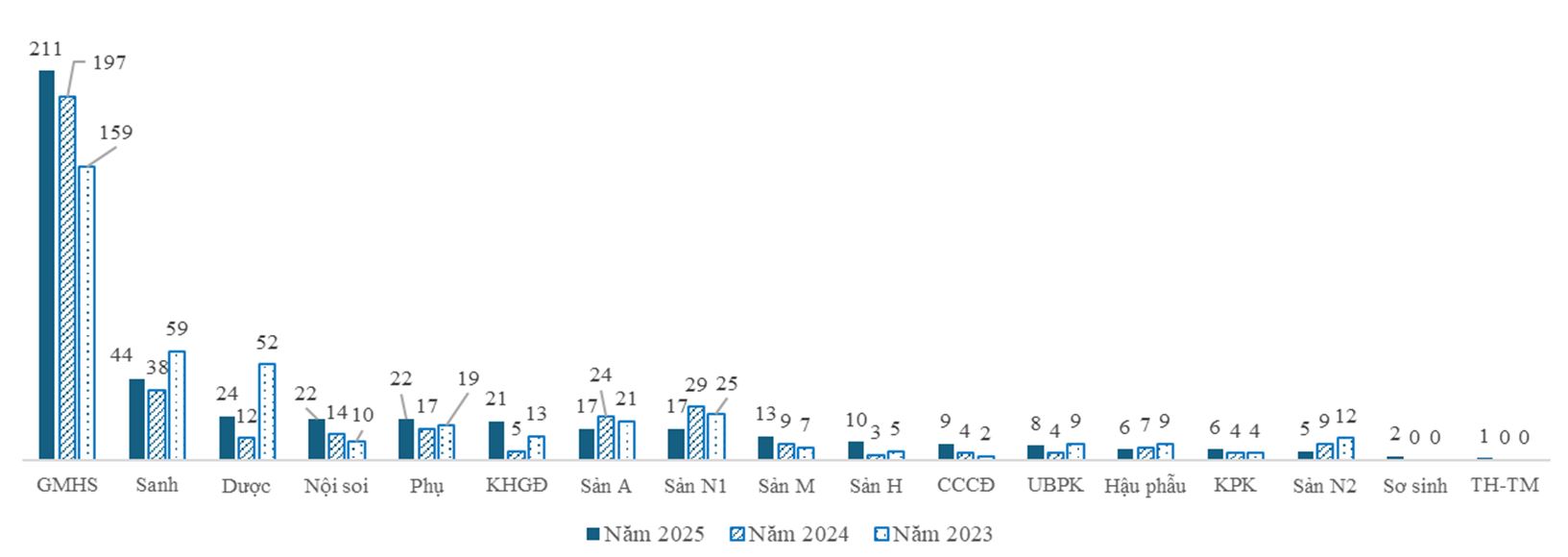
Hình 3. Số báo cáo ADR theo từng khoa/phòng trong 3 năm
Có sự biến động liên tục theo từng năm về số lượng báo cáo ADR ở các khoa lâm sàng:
- Khoa Gây mê hồi sức luôn có số lượng báo cáo cao nhất trong 03 năm 2023-2025 tại bệnh viện. Trong năm 2025, khoa có 211 báo cáo (chiếm tỉ lệ 48,2%) và tăng 1,1 lần so với năm 2024.
- Khoa Dược và khoa Sanh có sự giảm về số lượng báo cáo ADR năm 2024 so với năm 2023. Cụ thể, số lượng báo cáo ADR tại khoa Dược giảm 4,3 lần; khoa Sanh giảm 1,6 lần so với năm 2023.
- Trong 2 năm gần đây, số lượng báo cáo ADR ghi nhận được từ các khoa Sản A-B, Sản N1 và Nội soi có sự gia tăng nhẹ.
1.3. Phân bố báo cáo ADR theo người báo cáo
Đối tượng báo cáo ADR năm 2025 chủ yếu là Bác sĩ với tỉ lệ là 59,4% (260 báo cáo), đa phần được thực hiện bởi các Bác sĩ khoa Gây mê hồi sức với tỉ lệ là 81,2% (211 báo cáo).
Bảng 1. Số báo cáo ADR theo đối tượng báo cáo trong 3 năm
|
Đối tượng |
Tỷ lệ (%) năm 2025 |
Tỷ lệ (%) năm 2024 |
Tỉ lệ (%) năm 2023 |
|
Bác sĩ |
59,4 |
59,6 |
50,2 |
|
Hộ sinh |
35,2 |
36,7 |
36,1 |
|
Dược sĩ |
5,5 |
3,2 |
12,7 |
|
Kĩ thuật viên |
0,0 |
0,0 |
0,2 |
|
Cử nhân/ Điều dưỡng |
0,0 |
0,5 |
0,2 |
2. Phân loại báo cáo ADR trong năm 2025
2.1. Theo nhóm dược lý
Phân bố số báo cáo ADR theo nhóm dược lý trong năm 2025 được trình bày ở Bảng 2.
Bảng 2. Phân bố số báo cáo ADR theo nhóm dược lý
|
STT |
Nhóm thuốc |
Số báo cáo ADR |
Tỷ lệ (%) |
|
1 |
Kháng sinh |
221 |
50,5 |
|
2 |
Giảm đau, hạ sốt |
134 |
30,6 |
|
3 |
Thuốc điều trị ung thư |
34 |
7,8 |
|
4 |
Thuốc thúc đẻ, cầm máu sau đẻ |
29 |
6,6 |
|
5 |
Tác động lên quá trình đông máu |
3 |
0,7 |
|
6 |
Thuốc gây tê, gây mê |
3 |
0,7 |
|
7 |
Thuốc giãn cơ, giải giãn cơ |
3 |
0,7 |
|
8 |
Dung dịch dùng ngoài |
2 |
0,5 |
|
9 |
Không rõ nguyên nhân |
2 |
0,5 |
|
10 |
Thuốc kháng sinh, kháng nấm đặt âm đạo |
2 |
0,5 |
|
11 |
Dịch truyền |
1 |
0,2 |
|
12 |
Thuốc cản quang |
1 |
0,2 |
|
13 |
Thuốc chống nôn, ói |
1 |
0,2 |
|
14 |
Thuốc điều trị thiếu máu |
1 |
0,2 |
|
15 |
Vắc xin |
1 |
0,2 |
|
|
Tổng |
438 |
100 |
Kháng sinh là nhóm thuốc có tỷ lệ báo cáo ADR nhiều nhất, chiếm tỷ lệ 50,5% (221 báo cáo). Trong đó, hoạt chất cefazolin natri và cefotaxime natri có tỉ lệ báo cáo cao nhất, lần lượt là 40,3% (89 báo cáo) và 29,9% (66 báo cáo).
Tiếp theo là nhóm thuốc giảm đau hạ sốt chiếm tỷ lệ 30,6% (134 báo cáo). Trong đó, đa số là các báo cáo ADR liên quan đến hoạt chất diclofenac natri, với tỉ lệ 73,9% (99 báo cáo).
Các thuốc có tỉ lệ báo cáo ADR nhiều nhất, cũng là các thuốc có số lượng sử dụng nhiều nhất tại bệnh viện.
2.2. Theo nhóm thuốc có nguy cơ cao gây ADR
Có 65 báo cáo ADR xảy ra liên quan đến thuốc thuộc nhóm thuốc nguy cơ cao gây ADR. Trong đó, có 29 trường hợp ADR ghi nhận với thuốc điều trị ung thư nhờ việc tăng cường công tác khai thác thông tin ADR ở người bệnh tái nhập viện có hoá trị trước đó.
Bảng 3. Các báo cáo ADR của thuốc liên quan đến thuốc thuộc nhóm nguy cơ cao gây ADR
|
STT |
Thuốc gây ADR |
Số trường hợp |
Mức độ ảnh hưởng |
|
Thuốc gây tê, gây mê |
|||
|
1 |
Bupivacaine aguettant 5mg/ml (Bupivacaine) Lidocain BFS 200mg (Lidocain hydroclorid monohydrat) Fentanyl Braun (Fentanyl) |
1 |
Không nghiêm trọng |
|
2 |
Atropin (Atropin sulfat) |
1 |
Không nghiêm trọng |
|
3 |
Thuốc tiêm Fentanyl citrate (Fentanyl) |
1 |
Không nghiêm trọng |
|
Thuốc giãn cơ, giải giãn cơ |
|||
|
4 |
BFS-NEOSTIGMIN 0.5mg/ml (Neostigmin metylsulfat) |
1 |
Không nghiêm trọng |
|
5 |
Noveron (Rocuronium bromide) |
1 |
Đe doạ tính mạng |
|
6 |
Vinstigmin (Neostigmin methylsulfat) |
1 |
Không nghiêm trọng |
|
Thuốc điều trị ung thư và điều hòa miễn dịch |
|||
|
7 |
Bocartin 150mg/15ml (Carboplatin) |
6 |
2 báo cáo ở mức độ đe doạ tính mạng; 4 báo cáo ở mức độ không nghiêm trọng |
|
8 |
Abevmy 400mg/16ml (Bevacizumab) |
1 |
Không nghiêm trọng |
|
9 |
Anzatax 100mg/16,7ml (Paclitaxel) Cisplaton 10mg/20ml (Cisplatin) |
1 |
Không nghiêm trọng |
|
10 |
Avegra Biocad 400mg/16ml (Bevacizumab) Bocartin 150 (Caboplatin) Gemita 200mg (Gemcitabin) |
1 |
Không nghiêm trọng |
|
11 |
Bleomycin Bidiphar 15U (Bleomycin) Cisplaton 10mg/20ml (Cisplatin) Etoposid Bidiphar 100mg (Etoposid) |
1 |
Không nghiêm trọng |
|
12 |
Bocartin 150 (Carboplatin ) Canpaxel 100 (Paclitaxel) |
1 |
Không nghiêm trọng |
|
13 |
Methotrexat (Methotrexat) |
7 |
Không nghiêm trọng |
|
14 |
Gemita 1g (Gemcitabin HCl) |
4 |
Không nghiêm trọng |
|
15 |
Chemodox 20mg/10ml (Doxorubicin hydrochlorid) Abevmy 100 (Bevacizumab) |
1 |
Không nghiêm trọng |
|
16 |
Cosmegen Lyovac 500mcg (Dactinomycin) Etoposid Bidiphar (Etoposid) Methotrexat (Methotrexat) |
3 |
Không nghiêm trọng |
|
17 |
Endoprost 125 mcg/0.5ml (Carboprost tromethamin) |
1 |
Không nghiêm trọng |
|
18 |
Canpaxel 100 mg (Paclitaxel) |
2 |
Không nghiêm trọng |
|
Thuốc cản quang |
|||
|
19 |
Dotarem 0,5 mmol/ml (Acid gadoteric) |
1 |
Không nghiêm trọng |
|
Vắc xin |
|||
|
20 |
IMOJEV (Virus Viêm não Nhật Bản chủng SA14-14-2 tái tổ hợp, sống, giảm độc lực) VARILRIX 0.5ML 1DOSE (Virus thuỷ đậu sống giảm độc lực) |
1 |
Nhập viện/Kéo dài thời gian nằm viện |
|
Thuốc thúc đẻ, cầm máu sau đẻ |
|||
|
21 |
Atiglucinol 40mg (Phloroglucinol 40mg + Trimethyl phloroglucinol 0,04mg) |
1 |
Không nghiêm trọng |
|
22 |
Heraprostol 200mcg (Misoprostol) |
7 |
Không nghiêm trọng |
|
23 |
Methylergometrine maleat injection 0,2mg/ml Hemotocin 100mcg (Carbetocin) Vinphatoxin 10IU/ml (Oxytocin) |
1 |
Không nghiêm trọng |
|
24 |
Mifetone 200 mcg (Misoprostol) |
14 |
Không nghiêm trọng |
|
25 |
Vingomin (Methylergometrin maleat) |
3 |
Không nghiêm trọng |
|
26 |
Vinphatoxin 5IU/1ml (Oxytocin) |
1 |
Đe doạ tính mạng |
|
27 |
Trenzamin inj 500mg (Acid Tranexamic) Methylergometrine maleat injection 0,2mg/ml (Methyl ergometrin maleat) |
1 |
Đe doạ tính mạng |
2.3. Theo mức độ nghiêm trọng của phản ứng
Trong năm 2025, có 10 báo cáo ADR của Bệnh viện Từ Dũ ghi nhận ở mức độ đe doạ tính mạng (Bảng 4). Trong đó, ghi nhận 1/10 trường hợp xảy ra ADR nghi ngờ do thuốc Mifetone 200mcg (Misoprostol), người bệnh có tiền sử sử dụng thuốc Heraprostol 200mcg (Misoprostol) tại viện trong đợt điều trị trước nhưng không có triệu chứng bất thường.
|
Nhóm thuốc |
Số báo cáo ADR có mức độ đe doạ tính mạng |
Phân tích |
|
Kháng sinh |
3 |
3 báo cáo liên quan đến Cefazolin 1g (Cefazolin natri) |
|
Thuốc điều trị ung thư |
2 |
2 báo cáo liên quan đến Bocartin 150 (Carboplatin) |
|
Vắc xin |
1 |
1 báo cáo liên quan đến IMOJEV (Virus Viêm não Nhật Bản chủng SA14-14-2 tái tổ hợp, sống, giảm độc lực) + VARILRIX 0.5ML 1DOSE (Virus thuỷ đậu sống giảm độc lực) |
|
Thuốc thúc đẻ, cầm máu sau đẻ |
2 |
1 báo cáo liên quan đến Vinphatoxin 5IU/ml (Oxytocin) 1 báo cáo liên quan đến Mifetone 200mcg (Misoprostol) |
|
Thuốc giãn cơ, thuốc giải giãn cơ |
1 |
1 báo cáo liên quan đến Noveron (Atracurium) |
|
Dị nguyên không rõ loại |
1 |
01 báo cáo liên quan đến các thuốc sau: - Trenzamin inj 500mg (Acid Tranexamic) - Methylergometrine maleat injection 0,2mg/ml (Methyl ergometrin maleat) |
2.4. Theo tiền căn dị ứng thuốc
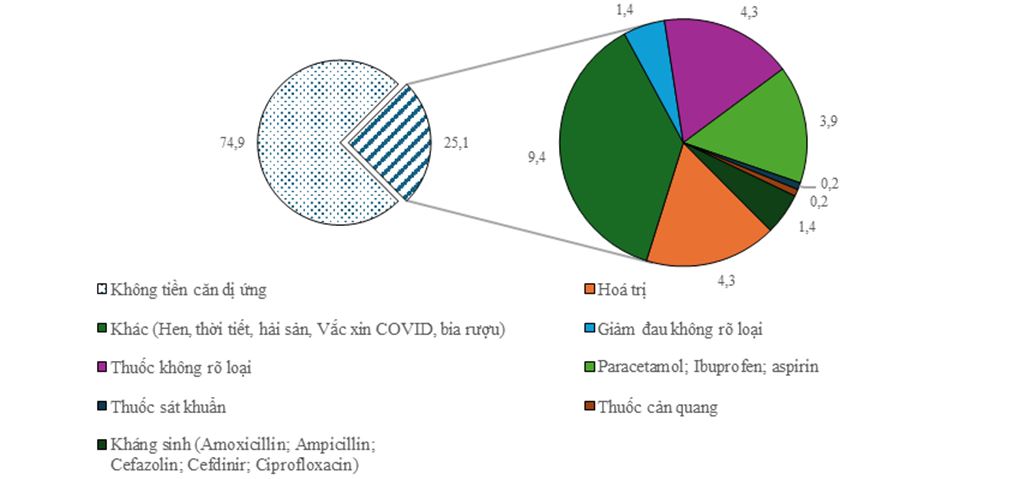
Hình 4. Phân bố báo cáo ADR theo tiền căn dị ứng thuốc
25,1% (110 báo cáo) có ghi nhận tiền căn dị ứng thuốc trên bệnh nhân. Phân tích các trường hợp xảy ra ADR trên những bệnh nhân có tiền căn dị ứng thuốc, 20,9% (23 báo cáo) ADR xảy ra trên những người bệnh đã cung cấp thông tin về tiền căn dị ứng thuốc không rõ loại, tỉ lệ này giảm 15,6% so với năm 2024 là 36,5% (35 báo cáo).
Một số trường hợp xảy ra ADR do chỉ định thuốc có chứa thành phần mà người bệnh đã cung cấp thông tin bản thân có tiền căn dị ứng (Bảng 5).
Bảng 5. ADR do chỉ định thuốc có chứa thành phần mà người bệnh đã cung cấp thông tin bản thân có tiền căn dị ứng
|
Thuốc gây ADR |
Tiền căn dị ứng |
Số trường hợp |
Triệu chứng |
Mức độ ảnh hưởng |
|
Thuốc giảm đau, hạ sốt |
||||
|
BV Ibugesic (Paracetamol + Ibuprofen) |
Dị ứng với Paracetamol nhưng không cung cấp thông tin khi NVYT khai thác tiền sử dị ứng |
1 |
Phù mí mắt dưới. |
Không nghiêm trọng |
|
Thuốc sát khuẩn |
||||
|
Povidon Iod 10% (Iodine) |
Tiền căn phản vệ phải nhập viện với thuốc sát khuẩn |
1 |
Sưng phù 2 mí mắt. |
Không nghiêm trọng |
3. Kết quả giám sát việc thực hiện quy trình giám sát phản ứng có hại của thuốc tại các khoa/phòng
Kết quả giám sát hoạt động theo dõi phản ứng có hại của thuốc từ tháng 01/2025 đến tháng 12/2025 theo “Quy trình giám sát phản ứng có hại của thuốc” (BVTD-QT-D-06), phiên bản 5.0 được phê duyệt ngày 21/12/2023: 96,11% (421/438 báo cáo) đạt tuân thủ thực hiện ở Bước 3 “Lập báo cáo ADR” (Bảng 6).
Bảng 6. Nội dung “Không đạt” theo quy trình “Giám sát phản ứng có hại của thuốc”
|
STT |
Nội dung thực hiện “Không đạt” |
Số lượng |
|
Bước 3 “Lập báo cáo ADR” |
||
|
1 |
Người báo cáo không ghi nhận thông tin về thuốc nghi ngờ gây ADR bao gồm: Tên thuốc gốc và tên thương mại, dạng bào chế, hàm lượng, nhà sản xuất, số lô, hạn dùng, liều dùng một lần, số lần dùng, đường dùng, ngày điều trị, lý do dùng thuốc. |
10 báo cáo |
|
2 |
Thiếu thông tin số lô thuốc |
03 báo cáo |
|
3 |
Sai thông tin số lô thuốc |
01 báo cáo |
|
4 |
Thiếu hàm lượng thuốc |
01 báo cáo |
|
5 |
Thiếu liều dùng |
01 báo cáo |
|
6 |
Không có thông tin người báo cáo ADR |
01 báo cáo |
Nhân viên chuyên trách của khoa Dược đã kịp thời bổ sung đầy đủ các thông tin cần thiết và phản hồi cho khoa lâm sàng trước khi tổng hợp các báo cáo gửi về Trung tâm DI & ADR quốc gia.
4. Kết quả giám sát thuốc kháng dị ứng tại các khoa lâm sàng
Kết quả giám sát thuốc kháng dị ứng và số lượng báo cáo ADR tại các khoa lâm sàng trong năm 2025 được trình bày trong Bảng 7.
Bảng 7. Kết quả giám sát thuốc kháng dị ứng tại các khoa lâm sàng
|
STT |
Khoa |
Số bệnh nhân sử dụng thuốc kháng dị ứng |
Số BN truyền máu |
Số báo cáo ADR |
||||
|
Chlorpheniramin |
Hydro-cortison |
Methyl-prednisolon |
Adrenalin |
Diphenhydramin |
||||
|
1 |
GMHS |
3 |
33 |
236 |
40 |
144 |
72 |
211 |
|
2 |
Khoa Sanh |
43 |
15 |
32 |
14 |
21 |
10 |
44 |
|
3 |
Sản A-B |
409 |
30 |
29 |
1 |
4 |
29 |
17 |
|
4 |
Khoa Phụ |
109 |
19 |
10 |
1 |
1 |
35 |
22 |
|
5 |
Sản N1 |
120 |
32 |
19 |
5 |
8 |
16 |
17 |
|
6 |
Hậu phẫu |
103 |
18 |
5 |
0 |
0 |
14 |
6 |
|
7 |
Sản N2 |
148 |
4 |
4 |
0 |
1 |
3 |
5 |
|
8 |
Sản M |
84 |
15 |
11 |
1 |
0 |
13 |
13 |
|
9 |
Nội soi |
188 |
19 |
3 |
0 |
0 |
8 |
22 |
|
10 |
THTM |
0 |
0 |
1 |
1 |
0 |
0 |
1 |
|
11 |
CCCĐ |
0 |
0 |
0 |
0 |
0 |
0 |
9 |
|
12 |
UBPK |
46 |
323 |
2538 |
4 |
1212 |
191 |
8 |
|
13 |
Sản H |
49 |
5 |
12 |
0 |
2 |
6 |
10 |
|
14 |
KHGĐ |
0 |
0 |
0 |
0 |
0 |
0 |
21 |
|
15 |
CSTS |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Xét một số thuốc xử trí phổ biến tại bệnh viện trong trường hợp xảy ra ADR, phần lớn có sự tương xứng giữa số lượng sử dụng adrenalin và diphenhydramin với số lượng báo cáo ADR tại mỗi khoa/phòng.
Đối với hydrocortison, kết quả phân tích sự tương xứng giữa số lượng báo cáo ADR với số lượng sử dụng tại các khoa lâm sàng được trình bày trong Bảng 8.
Bảng 8. Phân tích sử dụng hydrocortison tại các khoa lâm sàng năm 2025
|
STT |
Khoa sử dụng |
Phân tích sử dụng hydrocortison |
||||
|
Số lượng sử dụng |
Số BN truyền máu |
Báo cáo ADR |
Lý do khác* |
Có thể xảy ra ADR nhưng chưa thực hiện báo cáo** |
||
|
1 |
Hậu phẫu |
18 |
5 |
2 |
9 |
2 |
|
2 |
Gây mê hồi sức |
33 |
10 |
3 |
20 |
0 |
|
3 |
Nội soi |
19 |
1 |
5 |
9 |
4 |
|
4 |
Phụ |
19 |
5 |
5 |
7 |
2 |
|
5 |
Sản A-B |
30 |
8 |
5 |
13 |
4 |
|
6 |
Sản H |
5 |
1 |
3 |
0 |
1 |
|
7 |
Sản M |
15 |
2 |
3 |
8 |
2 |
|
8 |
Sản N1 |
32 |
7 |
11 |
9 |
5 |
|
9 |
Sản N2 |
4 |
0 |
1 |
2 |
1 |
|
10 |
Sanh |
15 |
1 |
2 |
11 |
1 |
* : Cường giáp, nhiễm độc giáp, lupus ban đỏ có/không biến chứng thận, bệnh lý đường hô hấp (hen suyển, hen phế quản, viêm phổi, suy hô hấp), ung thư, dính, tắc ruột,…
**: Xét các trường hợp đổi thuốc, ngưng thuốc sau khi dùng kháng dị ứng, sử dụng ≥ 02 thuốc dùng để xử trí ADR
Qua phân tích, cho thấy khoa Gây mê hồi sức có 33 BN sử dụng hydrocortison, là khoa có số lượng sử dụng hydrocortison cao thứ nhất tại bệnh viện. Khoa Sản N1 có 05/32 trường hợp, Sản A-B có 04/30 trường hợp và khoa Nội soi có 04/19 trường hợp có sử dụng hydrocortisol chưa tương ứng với số lượng báo cáo ADR..
5. Tóm tắt
- Số lượng báo cáo ADR của Bệnh viện Từ Dũ gửi về Đơn vị ADR tại Bệnh viện Từ Dũ trong năm 2025 là 438 báo cáo, tăng 15,9% so với năm 2024 và tăng 7,4% so với năm 2023.
- Trong đó, khoa Gây mê hồi sức, khoa Sanh và khoa Dược là 03 khoa có số ca báo cáo ADR cao nhất, với tỷ lệ lần lượt là: 48,2%, 10,1% và 5,5%.
- Kháng sinh là nhóm thuốc có tỉ lệ báo cáo ADR nhiều nhất: 50,5% (221 báo cáo). Trong đó, hoạt chất cefazolin natri và cefotaxime natri có tỉ lệ báo cáo cao nhất, lần lượt là 40,3% và 29,9%.



