Thông tin thuốc tháng 7/2025
Báo cáo ADR 6 tháng đầu năm 2025
I. Tình hình báo cáo ADR 6 tháng đầu năm 2025
Trong 6 tháng đầu năm 2025, Bệnh viện Từ Dũ ghi nhận 204 báo cáo ADR, tăng 1,3 lần so với cùng kỳ năm 2024 (160 báo cáo).
a) Số lượng báo cáo ADR phân bố theo tháng
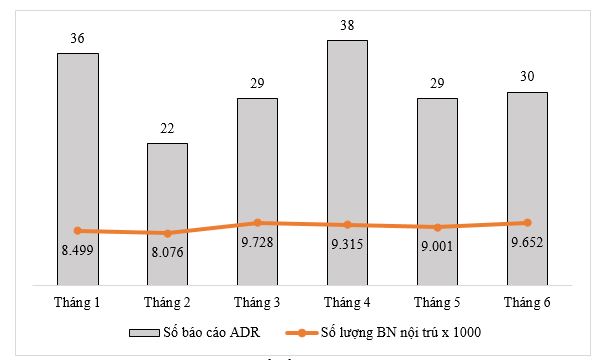
Hình 1. Sự phân bố số báo cáo ADR nội trú theo tháng
Số lượng báo cáo ADR nội trú trong năm 2025 phân bố theo tháng chưa tương ứng với số lượng bệnh của từng tháng (Hình 1). Tháng 2 có số lượng bệnh thấp nhất, đồng thời có số lượng báo cáo ADR cao nhất. Tuy nhiên, tháng 3 và tháng 6 có số lượng bệnh cao nhất, nhưng số lượng báo cáo ADR thấp hơn các tháng còn lại.
- 6 tháng đầu năm 2025: 1 báo cáo ADR thực hiện/295 người bệnh nội trú
- 6 tháng đầu năm 2024: 1 báo cáo ADR thực hiện/393 người bệnh nội trú
b) Số lượng báo cáo ADR phân bố theo khoa lâm sàng
|
Khoa lâm sàng |
6 tháng đầu năm 2025 |
6 tháng đầu năm 2024 |
|
Khối ngoại trú |
20 |
13 |
|
Khoa Kế Hoạch Gia Đình |
8 |
3 |
|
Khoa Dược |
6 |
7 |
|
Khoa Khám Phụ Khoa |
5 |
3 |
|
Khoa Khám trẻ - Sơ sinh |
1 |
0 |
|
Khối nội trú |
184 |
147 |
|
Khoa Gây Mê Hồi Sức |
106 |
82 |
|
Khoa Sanh |
21 |
18 |
|
Khoa Phụ |
14 |
9 |
|
Khoa Nội Soi |
12 |
3 |
|
Khoa Cấp Cứu Chống Độc |
7 |
2 |
|
Khoa Sản A-B |
6 |
10 |
|
Khoa Sản N1 |
5 |
8 |
|
Khoa Sản M |
5 |
4 |
|
Khoa Hậu Phẫu |
3 |
5 |
|
Khoa Ung Bướu Phụ Khoa |
3 |
2 |
|
Khoa Sản N2 |
2 |
4 |
|
Khoa Sản H |
0 |
0 |
|
Khoa Chẩn đoán hình ảnh |
0 |
0 |
Bảng 1. Phân bố số báo cáo ADR theo khoa lâm sàng
Nhận xét:
Khối ngoại trú:
- Số lượng báo cáo ADR từ khối ngoại trú là 20 báo cáo, tăng 1,5 lần so với cùng kỳ năm 2024 (13 báo cáo).
- Khoa Kế hoạch gia đình có số lượng báo cáo cao nhất (8 báo cáo), chiếm tỉ lệ 40,0% báo cáo ADR ngoại trú.
- Ghi nhận 1 báo cáo ADR từ khoa Khám trẻ - Sơ sinh, liên quan đến vắc xin.
Khối nội trú:
-Số lượng báo cáo ADR từ khối nội trú là 184 báo cáo, tăng 1,25 lần so với cùng kỳ năm 2024.
- Khoa GMHS có số lượng báo cáo cao nhất (106 báo cáo), chiếm tỉ lệ 57,6% báo cáo ADR nội trú.
- Không ghi nhận báo cáo ADR từ khoa Sản H, khoa Chẩn đoán hình ảnh.
c) Số lượng báo cáo ADR phân bố theo đối tượng báo cáo
|
Số báo cáo ADR |
Tỉ lệ (%) |
|
Bác sĩ |
129 |
63,2% |
Hộ sinh |
69 |
33,8% |
Dược sĩ |
6 |
3,0% |
Bảng 2. Phân bố số báo cáo ADR theo đối tượng báo cáo
Nhận xét: Đối tượng báo cáo ADR chủ yếu là Bác sĩ, với 129 báo cáo (chiếm tỉ lệ 63,2%), tỉ lệ này cao hơn 2,6% so với cùng kỳ năm 2024. Trong đó, 106/129 báo cáo (chiếm tỉ lệ 82,2%) là báo cáo từ các Bác sĩ khoa Gây mê hồi sức.
II. Thông tin về thuốc gây ADR trong 6 tháng đầu năm 2025
a) Theo nhóm dược lý
03 nhóm thuốc có số lượng báo cáo ADR cao nhất trong 6 tháng đầu năm 2025, bao gồm:
|
Nhóm thuốc |
Tỷ lệ số báo cáo ADR trên tổng số báo cáo (%) |
Phân tích |
|
Kháng sinh |
47,5% (97 báo cáo) |
- Hoạt chất cefazolin natri chiếm tỷ lệ cao nhất: 44,3% (43 báo cáo ADR), theo sau là cefotaxime natri chiếm tỷ lệ 26,8% (26 báo cáo ADR). - 92,8% (90 báo cáo ADR) liên quan đến nhóm kháng sinh β-lactam. |
|
Thuốc giảm đau, hạ sốt, chống viêm không steroid |
33,8% (69 báo cáo) |
- 89,9% (62 báo cáo ADR) liên quan đến nhóm thuốc giảm đau chống viêm không steroid (diclofenac, ibuprofen). - 7,2% (05 báo cáo ADR) liên quan đến paracetamol đường truyền. - 2,9% (02 báo cáo ADR) liên quan đến nefopam hydrochloride. |
|
Thuốc thúc đẻ, cầm máu sau đẻ |
4,9% (10 báo cáo) |
70,0% (07 báo cáo ADR) liên quan đến misoprostol đường đặt hậu môn, đường ngậm dưới lưỡi. |
Bảng 3. Phân bố tỷ lệ báo cáo ADR theo nhóm thuốc
Trong 6 tháng đầu năm 2025, có 10 trường hợp BN không xác định được nguyên nhân gây ADR. Trong đó, 4/10 trường hợp nghi ngờ có liên quan đến Cefotaxime 1g (Cefotaxime natri) thuộc nhóm thuốc kháng sinh.
b) Theo nhóm thuốc có nguy cơ cao gây ADR
Một số báo cáo ADR liên quan đến thuốc có nguy cơ cao gây ADR trong 6 tháng đầu năm 2025, bao gồm:
|
Hoạt chất |
Tên thành phẩm của thuốc |
Nhà sản xuất |
Số báo cáo ADR liên quan |
|
Methotrexate |
Methotrexat 25mg/1ml |
Công ty Cổ phần Dược - Trang thiết bị y tế Bình Định |
5 |
|
Carboplatin |
Bocartin 150mg/15ml |
Công ty Cổ phần Dược - Trang thiết bị Y tế Bình Định |
3 |
|
Oxytocin |
Vinphatoxin 5IU/ml |
Công ty cổ phần Dược phẩm Vĩnh Phúc |
1 |
|
Vinphatoxin 10IU/ml |
Công ty cổ phần Dược phẩm Vĩnh Phúc |
1 |
|
|
Methyl ergometrin maleat |
Methylergometrin maleat Injection 0,2mg/1ml |
Panpharma GmbH |
2 |
|
Vingomin 0,2mg/ml |
Công ty cổ phần dược phẩm Vĩnh Phúc |
2 |
|
|
Lidocain HCl |
Lidocain-BFS 200mg |
Công ty cổ phần dược phẩm CPC1 Hà Nội |
1 |
|
Rocuronium bromide |
Noveron 10mg/ml |
PT. Novell Pharmaceutical Laboratories |
1 |
|
Carbetocin |
Hemotocin 100mcg |
Công ty Cổ phần Dược phẩm CPC1 Hà Nội |
1 |
|
Bupivacaine hydrochloride |
Bupivacaine Aguettant 5mg/ml |
Delpharm Tours |
1 |
|
Fentanyl citrat |
Fentanyl B.Braun 0,1mg/2ml |
B.Braun Melsungen AG |
1 |
|
Acid gadoteric |
Dotarem 27,932g/100mL |
Guerbet |
1 |
|
Neostigmin metylsulfat |
BFS-Neostigmin 0,5mg/ml |
Công ty Cổ phần Dược phẩm CPC1 Hà Nội |
1 |
Bảng 4. Các báo cáo ADR của thuốc trong danh mục các thuốc thuộc nhóm nguy cơ cao gây ADR
Trong 6 tháng đầu năm 2025, ghi nhận 5/21 trường hợp báo cáo ADR với thuốc có nguy cơ cao gây ADR với Methotrexat 25mg/ml, ở mức độ không nghiêm trọng với các triệu chứng: loét miệng, nhìn mờ thoáng qua.
c) Theo mức độ đe doạ tính mạng
Trong 6 tháng đầu năm 2025, có 09 báo cáo ADR của Bệnh viện Từ Dũ ghi nhận ở mức độ đe doạ tính mạng và 01 báo cáo ADR ở mức độ nhập viện/ kéo dài thời gian nằm viện (Bảng 5). Trong 10 báo cáo ADR ở mức độ nghiêm trọng đã được ghi nhận, có 03 báo cáo có liên quan đến thuốc có nguy cơ cao gây ADR, bao gồm: Noveron 10mg/ml (Rocuronium bromide); Vinphatoxin 5IU/ml (Oxytocin); Methylergometrine maleat injection 0,2mg/ml (Methylergometrin maleat).
|
Nhóm thuốc |
Số báo cáo ADR có mức độ đe doạ tính mạng |
Phân tích |
|
Kháng sinh |
4 |
100% các báo cáo ADR liên quan đến kháng sinh đều là kháng sinh nhóm β-lactam: - Cefazolin 1g (Cefazolin natri): 1 báo cáo - Cefazolin 2g (Cefazolin natri): 1 báo cáo - Zoliicef 1g (Cefazolin natri): 2 báo cáo |
|
Thuốc giãn cơ, giải giãn cơ |
1 |
1 báo cáo liên quan đến Noveron 10mg/ml (Rocuronium bromide) |
|
Thuốc giảm đau, hạ sốt, chống viêm không steroid |
1 |
1 báo cáo liên quan đến Acupan (Nefopam hydrochloride) |
|
Thuốc thúc đẻ, cầm máu sau đẻ |
1 |
1 báo cáo liên quan đến Vinphatoxin 5IU/ml (Oxytocin) |
|
Dị nguyên không rõ loại |
2 |
1 báo cáo liên quan đến các thuốc: - Diclofenac 100mg (Diclofenac natri) - Cefotaxime 1g (Cefotaxime natri) - Gentamicin 80mg/2ml (Gentamicin sulfat) 1 báo cáo liên quan đến các thuốc: - Trenzamin inj 500mg (Acid tranexamic) - Methylergometrine maleat injection 0,2mg/ml (Methylergometrin maleat) |
Bảng 5. Các báo cáo ADR ở mức độ đe doạ tính mạng được báo cáo
d) Theo tiền căn dị ứng thuốc
Trong 6 tháng đầu năm 2025, 15,7% (32 báo cáo) ghi nhận BN có tiền căn dị ứng thuốc. Phân tích các trường hợp xảy ra ADR trên những BN có tiền căn dị ứng, đa phần người bệnh cung cấp thông tin là có tiền căn dị ứng thuốc không rõ loại, tỉ lệ 46,9% (15 báo cáo).
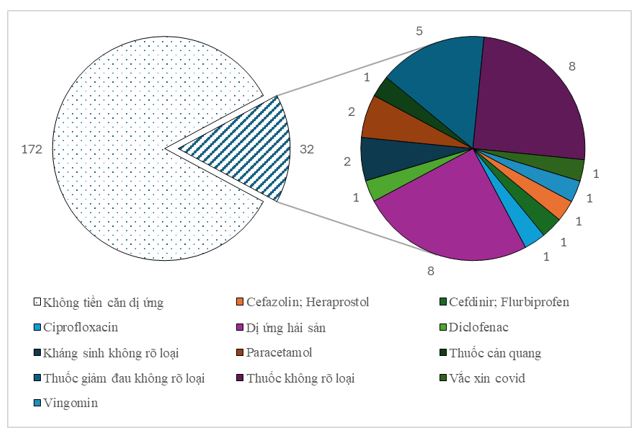
Hình 2. Phân bố báo cáo ADR theo tiền căn dị ứng thuốc
III. Kết quả giám sát việc thực hiện quy trình giám sát phản ứng có hại của thuốc tại các khoa/phòng
Kết quả giám sát hoạt động theo dõi phản ứng có hại của thuốc từ tháng 01/2025 đến tháng 6/2025 theo “Quy trình giám sát phản ứng có hại của thuốc” (BVTD-QT-D-06), phiên bản 5.0 được phê duyệt ngày 21/12/2023: 97,1% (198/204 báo cáo) đạt tuân thủ thực hiện ở Bước 3 “Lập báo cáo ADR” (Bảng 6).
|
STT |
Nội dung thực hiện “Không đạt” |
Số lượng |
|
Bước 3 “Lập báo cáo ADR” |
||
|
1 |
Người báo cáo không nêu đầy đủ thông tin về thuốc nghi ngờ gây ADR bao gồm: Tên thuốc gốc và tên thương mại, dạng bào chế, hàm lượng, nhà sản xuất, số lô, hạn dùng, liều dùng một lần, số lần dùng, đường dùng, ngày điều trị, lý do dùng thuốc. |
04 báo cáo |
|
2 |
Thiếu thông tin số lô thuốc |
02 báo cáo |
Bảng 6. Nội dung thực hiện “Không đạt” theo quy trình “Giám sát phản ứng có hại của thuốc”
Nhân viên chuyên trách của khoa Dược đã kịp thời bổ sung đầy đủ các thông tin cần thiết và phản hồi cho khoa lâm sàng trước khi tổng hợp các báo cáo gửi về Trung tâm DI & ADR quốc gia.
IV. Kết quả giám sát thuốc kháng dị ứng tại các khoa lâm sàng
Kết quả giám sát thuốc kháng dị ứng và số lượng báo cáo ADR trong 6 tháng đầu năm 2025 được trình bày ở Bảng 7.
|
STT |
Khoa |
Số bệnh nhân sử dụng thuốc kháng dị ứng |
Số BN truyền máu |
Số báo cáo ADR |
||||
|
Chlorpheniramin |
Hydro-cortison |
Methyl-prednisolon |
Adrenalin |
Diphenhydramin |
||||
|
1 |
GMHS |
1 |
14 |
113 |
16 |
20 |
24 |
106 |
|
2 |
Khoa Sanh |
8 |
7 |
18 |
9 |
0 |
5 |
21 |
|
3 |
Khoa Phụ |
43 |
11 |
12 |
1 |
0 |
18 |
14 |
|
4 |
Nội soi |
73 |
12 |
6 |
0 |
0 |
4 |
12 |
|
5 |
CCCĐ |
0 |
0 |
0 |
0 |
0 |
0 |
7 |
|
6 |
Sản A-B |
159 |
16 |
32 |
1 |
1 |
12 |
6 |
|
7 |
Sản M |
26 |
6 |
46 |
0 |
0 |
8 |
5 |
|
8 |
Sản N1 |
64 |
20 |
13 |
0 |
1 |
10 |
5 |
|
9 |
Hậu phẫu |
47 |
11 |
3 |
0 |
0 |
6 |
3 |
|
10 |
UBPK |
16 |
147 |
1713 |
2 |
288 |
60 |
3 |
|
11 |
Sản N2 |
75 |
2 |
4 |
0 |
0 |
1 |
2 |
|
12 |
KPK |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
13 |
Sản H |
20 |
3 |
5 |
0 |
0 |
4 0 |
0 |
|
14 |
KHGĐ |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
15 |
CSTS |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
16 |
CĐHA |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
Bảng 7. Kết quả giám sát thuốc kháng dị ứng tại các khoa lâm sàng trong 6 tháng đầu năm 2025
Xét một số thuốc xử trí phổ biến tại bệnh viện trong trường hợp xảy ra ADR, đa số có sự tương xứng giữa số lượng báo cáo ADR với số lượng BN sử dụng diphenhydramin, adrenalin. Đối với hydrocortison, kết quả phân tích sự tương xứng giữa số lượng báo cáo ADR với số lượng BN sử dụng tại khoa lâm sàng được trình bày trong Bảng 8.
|
STT |
Khoa sử dụng |
Phân tích sử dụng hydrocortison |
|||
|
Số lượng BN sử dụng |
Số BN truyền máu |
Báo cáo ADR |
Lý do khác* |
||
|
1 |
Sản N1 |
20 |
6 |
4 |
6 |
|
2 |
Sản A-B |
16 |
5 |
1 |
8 |
|
3 |
Gây mê hồi sức |
14 |
6 |
1 |
7 |
|
4 |
Nội soi |
12 |
1 |
4 |
3 |
|
5 |
Phụ |
11 |
4 |
2 |
3 |
|
6 |
Hậu phẫu |
11 |
3 |
1 |
6 |
|
7 |
Sanh |
7 |
1 |
1 |
5 |
|
8 |
Sản M |
6 |
1 |
1 |
3 |
|
9 |
Sản N2 |
2 |
0 |
0 |
1 |
|
10 |
Sản H |
3 |
1 |
1 |
0 |
* : Cường giáp, nhiễm độc giáp, lupus ban đỏ có/không biến chứng thận, bệnh lý đường hô hấp (hen suyển, hen phế quản), sốc nhiễm trùng,…
Bảng 8. Phân tích sử dụng hydrocortison tại các khoa lâm sàng trong 6 tháng đầu năm 2025
Theo kết quả phân tích, khoa Nội soi và khoa Sản N1 số lượng sử dụng hydrocortison không tương xứng với số lượng báo cáo ADR trong 6 tháng đầu năm 2025. Trong đó, khoa Sản N1 cũng là khoa có kết quả sử dụng hydrocortison không tương xứng với số lượng báo cáo ADR trong cùng kỳ năm 2024.
V. Tóm tắt
- Số lượng báo cáo ADR trong 6 tháng đầu năm 2025 tăng 1,3 lần so với cùng kỳ năm 2024.
- Số lượng báo cáo ADR đối với thuốc có nguy cơ cao gây ADR trong 6 tháng đầu năm 2025 tăng 1,6 lần so với cùng kỳ năm 2024.
- Kháng sinh là nhóm thuốc được báo cáo ADR và gây ADR đe dọa tính mạng cao nhất, với tỉ lệ lần lượt là 47,5% và 44,4%.



