Kháng sinh Ertapenem có thua kém các kháng sinh carbapenem khác trong điều trị nhiễm trùng do Escherichia coli (E. coli) sinh ESBL?
Carbapenem là khuyến cáo đầu tay điều trị nhiễm trùng ngoài đường tiết niệu do Enterobacterales sinh ESBL (ESBL-E) gây ra (5). Ertapenem là Carbapenem nhóm 1 được chỉ định điều trị nhiễm trùng gram âm đa kháng (không bao gồm Pseudomonas và Acinetobacter).
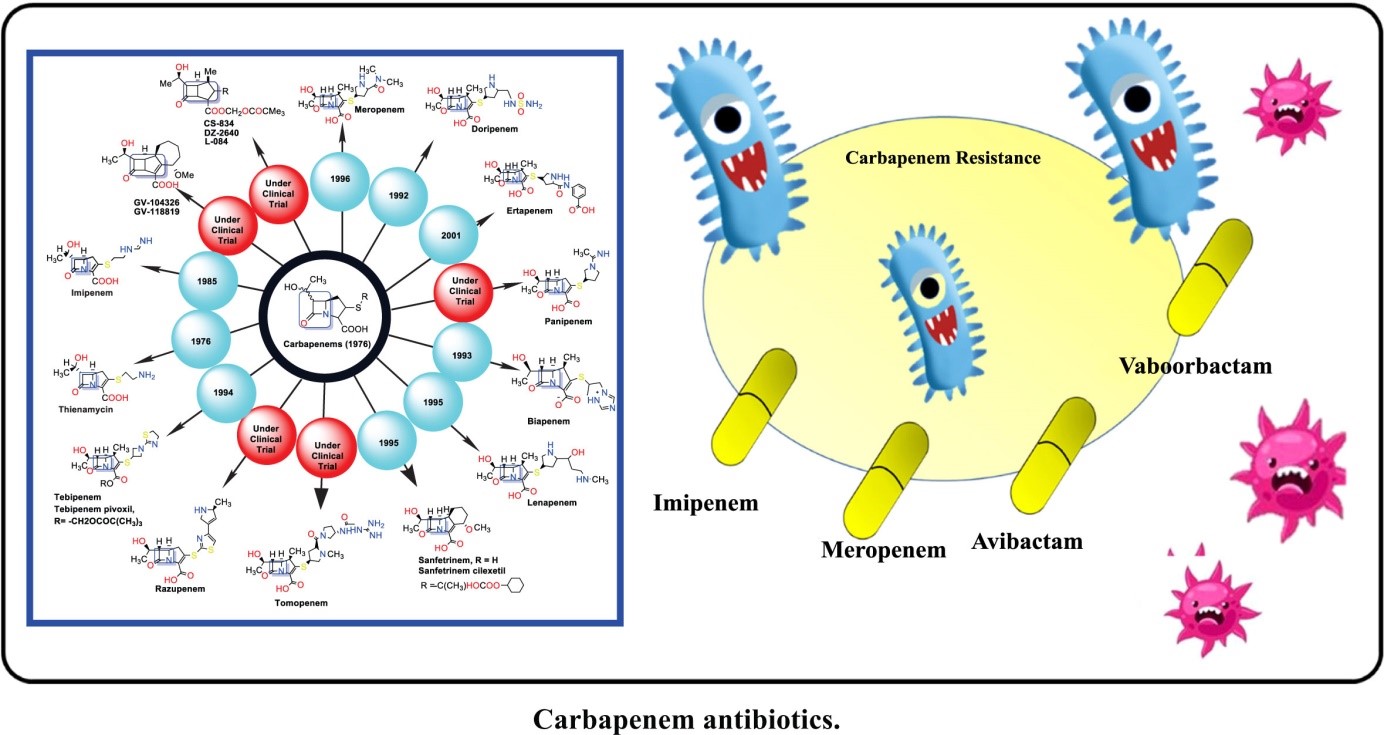
Hình 1. Lịch sử hình thành của các kháng sinh nhóm carbapenem (1)
Ưu điểm: Ertapenem là kháng sinh mới nhất trong các kháng sinh carbapenem đang sử dụng trên lâm sàng, khả năng gắn kết cao với protein (95%), dẫn đến thời gian bán thải tương đối kéo dài, là kháng sinh duy nhất trong nhóm carbapenem dùng liều 1 lần/ngày (5).
Nhược điểm: So với các carbapenem khác, Ertapenem có hoạt tính rất kém đối với vi khuẩn Enterococcus, Pseudomonas aeruginosa và Acinetobacter baumannii. Đối với bệnh nhân nặng và có giảm albumin máu, phần tự do của Ertapenem tăng, dẫn đến giảm đáng kể thời gian bán thải thuốc, giảm hiệu quả điều trị.
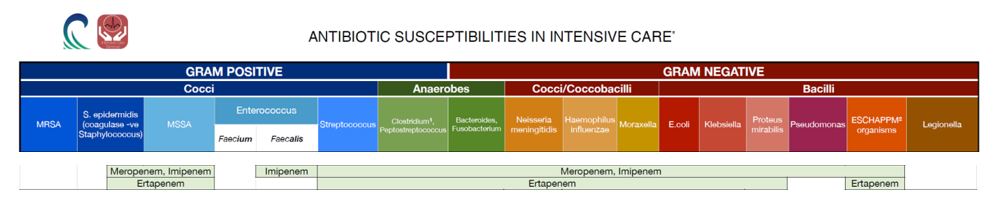
Một nghiên cứu đoàn hệ hồi cứu đa quốc gia (dự án INCREMENT) đã được thực hiện từ tháng 01 năm 2004 đến tháng 12 năm 2013, với 37 bệnh viện của 12 quốc gia đã tham gia, nghiên cứu trên 509 bệnh nhân nhiễm trùng, trong đó 205 bệnh nhân được điều trị bằng Ertapenem và 304 bằng carbapenem khác (Meropenem:185, imipenem:118 và doripenem:1). Nhiễm trùng tiết niệu và nhiễm trùng do E. coli thường gặp hơn ở những bệnh nhân được điều trị bằng Ertapenem, nhiễm trùng bệnh viện, ung thư và nhiễm trùng huyết/sốc nhiễm trùng ít gặp hơn. Không có sự khác biệt về loại ESBL giữa nhóm được điều trị bằng Ertapenem và nhóm điều trị bằng carbapenem khác. Phác đồ liều được sử dụng là: Imipenem 500 mg mỗi 6 giờ (49,1%); Meropenem 1 g mỗi 8 giờ (50,8%); và Ertapenem 1g 1 lần/ngày (84,3%). Liều đã được hiệu chỉnh ở bệnh nhân suy thận. Kết quả nghiên cứu ủng hộ mạnh mẽ giả thuyết Ertapenem có hoạt tính không thua kém các carbapenem khác trong điều trị nhiễm trùng huyết do ESBL-E, mặc dù cần có thêm dữ liệu cho các nhóm bệnh nhân cụ thể. Điều quan trọng là những dữ liệu này gợi ý rằng Ertapenem nếu có hoạt tính in vitro, có thể được sử dụng thay cho carbapenem phổ rộng hơn, để điều trị nhiễm trùng huyết do ESBL-E trong nhiều tình huống lâm sàng (2).
Bảng. MIC Ertapenem đối với Enterobacteriaceae (3)
|
Nhạy (S) |
Trung gian (I) |
Kháng (R) |
|
≤ 0,5 mcg/mL |
1 mcg/mL |
≥ 2mcg/mL |
Nghiên cứu tổng quan hệ thống của tác giả Huang và cộng sự năm 2023 cho kết quả: Ertapenem có hiệu quả điều trị tương tự như các carbapenem khác (hầu hết các trường hợp trong nghiên cứu là nhiễm trùng máu thứ phát từ nhiễm trùng đường niệu hoặc đường mật do ESBL-E, chưa có dữ liệu trên nhiễm trùng huyết nặng, sốc nhiễm trùng hoặc nhiễm trùng suy đa tạng). Thứ nhất, tỉ lệ tử vong ở nhóm ertapenem tương tự với các nhóm carbapenem khác. Thứ hai, ertapenem có liên quan đến thời gian nằm viện ngắn hơn so với các carbapenem khác. Thứ ba, tỷ lệ cải thiện và chữa khỏi lâm sàng, tỷ lệ vi khuẩn được loại bỏ là tương tự nhau giữa ertapenem và các nhóm carbapenem khác. Nhìn chung, những phát hiện này cho thấy hiệu quả rõ ràng của ertapenem trong điều trị nhiễm trùng do Enterobacterales sinh ESBL (4).
Ertapenem có thể được sử dụng như một liệu pháp xuống thang đối với các bệnh nhiễm trùng ESBL-E?
Nghiên cứu của tác giả Pinyo Rattanaumpawan và cộng sự từ tháng 6 năm 2011 đến tháng 12 năm 2014, với 32 bệnh nhân được chọn ngẫu nhiên vào nhóm xuống thang (là những người đang dùng bất kỳ loại carbapenem nhóm 2 nào (imipenem, meropenem, doripenem) trong vòng chưa đầy 96 giờ và được xuống thang bằng ertapenem) và 34 bệnh nhân thuộc nhóm chứng. Vị trí nhiễm trùng phổ biến nhất là nhiễm trùng đường tiết niệu (42%). Đặc điểm của cả hai nhóm được so sánh. Bằng cách sử dụng biên độ xác định trước 15%, ertapenem không thua kém nhóm chứng về tỷ lệ khỏi bệnh trên lâm sàng (%Δ = 14,0 [khoảng tin cậy 95%:-2,4 đến 31,1]), tỷ lệ loại bỏ vi sinh vật (%Δ = 4,1 [-5,0 đến 13,4]) và tỷ lệ lây nhiễm cộng dồn (%Δ =-16,5 [-38,4 đến 5,3]). Bệnh nhân trong nhóm xuống thang có tỷ lệ tử vong trong 28 ngày thấp hơn có ý nghĩa (9,4% so với 29,4%; P = 0,05), thời gian nằm viện trung bình ngắn hơn có ý nghĩa (16,5 ngày [4,0–73,25] so với 20,0 ngày [1,0–112,25]; P = 0,04) và liều sử dụng carbapenem hàng ngày được xác định thấp hơn có ý nghĩa (12,9 ± 8,9 so với 18,4 ± 12,6; P = 0,05). Do đó, Ertapenem có thể được sử dụng một cách an toàn như một liệu pháp xuống thang đối với các bệnh nhiễm trùng Enterobacteriaceae sinh ESBL, khi đã biết được độ nhạy cảm. Các nghiên cứu trong tương lai là cần thiết để nghiên cứu hiệu quả của ertapenem đối với bệnh viêm phổi do ESBL-E để xác định khả năng ứng dụng của nó trong các tình trạng đe dọa đến tính mạng (6).
Ertapenem có ảnh hưởng đến tính nhạy cảm của vi khuẩn đối với các Carbapenem khác không?
Nghiên cứu hồi cứu thực hiện tại một bệnh viện Nam California đã nghiên cứu về việc sử dụng kháng sinh ertapenem và tính nhạy cảm của Pseudomonas aeruginosa từ tháng 01 năm 2022 đến tháng 12 năm 2005. Xu hướng tăng tính nhạy cảm của P. aeruginosa với imipenem, cefepime và Piperacillin/Tazobactam đã được ghi nhận. Có thể liên quan đến việc tăng sử dụng ertapenem và giảm sử dụng imipenem. Trong khi việc tăng sử dụng carbapenem nhóm 2 đã dẫn đến sự xuất hiện của P. aeruginosa kháng imipenem. Theo số liệu thống kê trong tháng, cứ giảm một đơn vị DDD (Tiêu thụ kháng sinh tính theo liều dùng một ngày) của Imipenem thì tính nhạy cảm của P. aeruginosa với imipenem tăng 0,38%. Không có sự thay đổi tính nhạy cảm ở các vi khuẩn E. coli, Proteus mirabilis, Klebsiella spp. hoặc Enterobacter cloacae, các mầm bệnh vẫn nhạy cảm 100% với ertapenem. Vì vậy, việc sử dụng Ertapenem phù hợp với dịch tể của cơ sở điều trị giúp cải thiện tổng thể hệ sinh thái bệnh viện trong một số trường hợp được báo cáo.
Do đó, nghiên cứu đề xuất Ertapenem nên được sử dụng như kháng sinh điều trị kinh nghiệm cho các bệnh nhiễm trùng do vi khuẩn gram âm hiếu khí và kỵ khí, vi khuẩn sinh ESBL hoặc nhiễm trùng ổ bụng phức tạp, với khả năng mắc Pseudomonas thường khó có thể xảy ra, dựa trên tiền sử dùng thuốc, các thông số lâm sàng và nhân khẩu học của người bệnh. (7)
Tài liệu tham khảo
(1) Tiwari Abhishek*, Tiwari Varsha, Sahoo Mohan Biswa, Banik Krishna Bimal, Kumar Manish and Verma Navneet, Carbapenem Antibiotics: Recent Update on Synthesis and Pharmacological Activities, Current Drug Research Reviews 2023; 15(1)
(2) REIPI/ESGBIS/INCREMENT Group. Ertapenem for the treatment of bloodstream infections due to ESBL-producing Enterobacteriaceae: a multinational pre-registered cohort study. J Antimicrob Chemother. 2016 Jun;71(6):1672-80.
(3) CLSI M100-ED33:2023 Performance Standards for Antimicrobial Susceptibility Testing, 33rd Edition.
(4) Huang, P.Y., Hsu, C.K., Liu, T.H., Wu, J.Y., Tang, H.J., Tsai, Y.W., Lai, C.C. and Chang, Y.H., 2023. Clinical efficacy of ertapenem versus other carbapenems for the treatment of extended-spectrum-β-lactamase-producing Enterobacterales infection: A systematic review and meta-analysis. Journal of Global Antimicrobial Resistance.
(5) AMR Guidance 3.0 – Updated 06/7/2023.
(6) Rattanaumpawan, P., Werarak, P., Jitmuang, A., Kiratisin, P. and Thamlikitkul, V., 2017. Efficacy and safety of de-escalation therapy to ertapenem for treatment of infections caused by extended-spectrum-β-lactamase-producing Enterobacteriaceae: an open-label randomized controlled trial. BMC Infectious Diseases, 17(1), pp.1-8.
(7) Nicolau, D.P., Carmeli, Y., Crank, C.W., Goff, D.A., Graber, C.J., Lima, A.L.L. and Goldstein, E.J., 2012. Carbapenem stewardship: does ertapenem affect Pseudomonas susceptibility to other carbapenems? A review of the evidence. International journal of antimicrobial agents, 39(1), pp.11-15.



